Европейската агенция по лекарствата (ЕМА) не може да потвърди от наличните данни дали жените и младите възрастни са изложени на по-висок риск от редки кръвни съсиреци с ниски тромбоцити след ваксинация с препарата на британско-шведската фармацевтична компания AstraZeneca срещу COVID-19, информира "Ройтерс".
Ограничения в начина на събиране на данните означавали, че EMA не може да идентифицира някакъв специфичен рисков фактор, който да прави състоянието, тромбоза със синдром на тромбоцитопения, по-вероятно, уточниха от агенцията.
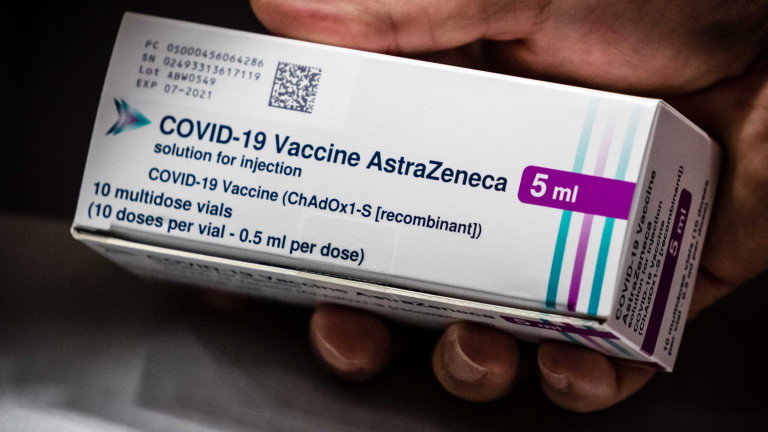
Европейската комисия поиска научно мнение от ЕМА след съобщения по-рано тази година за тромбоза със синдром на тромбоцитопения, свързани с ваксината, което накара много държави от ЕС да преустановят използването на препарата, по-рано разглеждан за ключов за плановете за имунизация в Общността.
EMA отбеляза, че повтаря, че втората доза от двудозовата ваксина, разработена заедно с Оксфордския университет, продължава да се прилага между четири и 12 седмици след първата.
"Няма доказателства, че забавянето на втората доза има някакво влияние върху риска от тромбоза със синдром на тромбоцитопения", увериха от EMA.
Агенцията също така изтъкна, че понастоящем не могат да бъдат дадени окончателни препоръки за използването на различна ваксина за втора доза след първа с препарата на AstraZeneca.









































 USD
USD CHF
CHF EUR
EUR GBP
GBP





























GolaVoda
на 17.09.2021 в 16:23:41 #3Американците събират информация в системата VAERS но медицинският бизнес отказва да ги анализира по простата причина, че ако го направи ще се формира прецедент и съдилищата ще се удавят.. Засега недоволството се удържа чрез страха насаждан в медиите и чрез пиар пропогандата от масирани поръчани научни изследвания, но рано и късно този преграда няма да издържи. . Вижте как стоят вещата в науката!!! тово неуките не го знаят!! ако вие напишете нещо което защитите с превдо-научви доводи.... то там вече им достатъмно доводи то да бъде оборено.. и тогава вашите конкуренти в науката виждат, че вие сте уязвим и посочват вашите проблеми.. защо вие да станете професор и да получите пари а те не??? голямата фармацевтика не може да нахрани всички, а и не иска да го прави. затова е мното важно наука да не се полза, а недоказани твърдения от тип АЗ ВЯРВАМ!! но живота си тече.
GolaVoda
на 17.09.2021 в 16:14:20 #2Смъкнах данните от американската система за рапортувания на оплаквания от ваксини. VAERS https://vaers.hhs.gov/eSubDownload/index.jsp?fn=2021VAERSVAX.csv Системата има 39 милиона оплаквания от различни ваксини за различни болести. От тях за ковид ваксините оплакванията са 560 000 броя и са от различен тип ефекти Ако ви се занимава може да си ги смъкнете и вие да се упражнявате в ексел. С български данни разбира се не можете да направите такова нещо не само, защото тези данни са строго конфиденциални и "събрани и обработени неизвестно как" но и защото на никой не му пука и не са му нужни!!! Не му пука, тъй като подписвате декларация, че каквото и да стане вие сам сте си виновен и никой друг не ви е виновен. Медицинската гилдия в САЩ отказва да анализира данните..те по принцип са зависими от голямата фармация.. Но не могат да откажат същестуваването на такава система защото там много неща минават през съдилищата.
ce
на 17.09.2021 в 16:11:51 #1>>> Ограничения в начина на събиране на данните означавали, че EMA не може да идентифицира някакъв специфичен рисков фактор Те уж с да кажат нещо положително за астрата, ама всъщност казаха истината за всички ваксини Не се събира никаква информация за нищо свързано с ваксините А още повече разделено по различен тип ваксина Това е огромен проблем който бива тотално игнориран